- HOME
- 진료안내
- 진료지원부서
- 약제부
진료지원부서
약제부- 듀드리진시럽 약품 회수 사실 안내
현재 본원에서 사용 중인 듀드리진 시럽 (Hydroxyzine HCl 2㎎/㎖)에 대해 의약품 회수 안내드립니다.
일부 제조번호에서 표시사항 중 원료의약품 분량의 오기(100mL를 30mL 표시)로 인한 해당 제조사의 자발적 회수가 진행 중입니다.
주요 사항:
- 회수 사유: 일부 제품의 표시사항 중 원료의약품 분량의 오기(100mL를 30mL 표시)로 인한 영업자 회수
- 회수 대상 제조번호 및 유효일자:
- 24002[2026-02-04]
업체명 제품명 제조번호[유효기간] 회수사유 삼아제약
두드리진시럽
24002[2026-02-04]
표시사항 중 원료의약품 분량의 오
(100mL를 30mL 표시)로 인한 영업자 회수
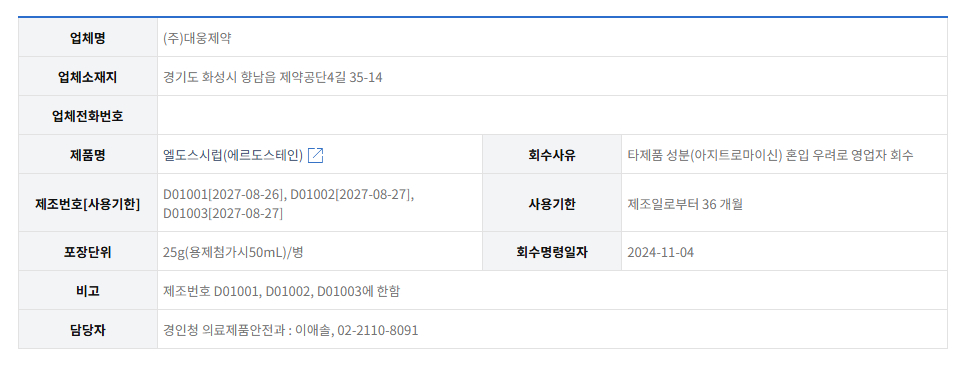
- 엘도스시럽 의약품 회수 사실 안내
1. 본원에서 사용중인 엘도스시럽 (대웅)에 대한 의약품 회수 사실안내 입니다.
2. 일부 제조번호에서 타제품성분 (아지트로마이신) 혼입 우려로 으로 인한 영업자 회수입니다.
3. 회수대상 의약품의 제조번호 [유효일자] 는 다음과 같습니다
D01001[2027-08-26], D01002[2027-08-27], D01003[2027-08-27]
4. 다른 제조번호 제품의 경우 사용 가능합니다.
- 신규사용알림 - 폭세틴캡슐 20mg (환인제약)
안녕하세요 노원을지병원 약제부입니다.
푸로작캡슐 20mg의 공급이 중단됨에 따라, 대체약품으로 폭세틴캡슐 20mg (환인제약)을 사용하게 되었음을 안내드립니다.
관련문의 : 약품관리실 (02-970-8384)
감사합니다.
시행예정일 : 24.09.13
성분명
코드
처방명
수가
제조/판매
구분
20㎎ as fluoxetine
657200990
폭세틴캡슐 20mg
262원
환인제약
대체사용
- 신규약품 사용알림 : 3품목
신규약품 사용을 알려드립니다.
제품코드 성분명 한글명 제약회사 보험가 분류번호 분류별 641106200 finerenone 10㎎ 케렌디아정10mg 바이엘코리아 1,670 219 신장병치료제 641106190 finerenone 20㎎ 케렌디아정20mg 바이엘코리아 1,670 219 신장병치료제 624900570 atogepant 60mg 아큅타정60mg 한국애브비 비급여 399 편두통 치료제 시행일시 : 24.8월 중
관련문의 : 약품관리실 (02-970-8384) 김명진
감사합니다.
- 의약품 회수 알림- 아킨지오캡슐 300/0.5mg
1. 본원에서 사용중인 아킨지오캡슐 300/0.5mg에 대한 의약품 회수 사실안내입니다.
2. 일부 제조번호에서 일부 주성분(팔로노세틑론염산염)의 함량 미달 가능성으로 인한영업자 회수입니다.
3. 회수대상 의약품의 제조번호 [유효일자] 는 다음과 같습니다
4. 다른 제조번호 제품의 경우 문제 없이 사용 가능합니다.
업체명 제품명 제조번호[유효기간] 회수사유 HK이노엔
아킨지오 캡슐
43000563[2026-11-30]]
일부 주성분(팔로노세틑론염산염)의 함량 미달 가능성
- 의약품 회수 알림- 카슈트현탁액 5g/20ml
1. 본원에서 사용중인 카슈트현탁액 5g/20ml에 대한의약품 회수 사실안내입니다.
2. 일부 제조번호에서 품질부적합 (미생물한도)기준 초과로 인한 영업자 회수입니다.
3. 회수대상 의약품의 제조번호 [유효일자] 는 다음과 같습니다
4. 다른 제조번호 제품의 경우 문제 없이 사용 가능합니다.
업체명 제품명 제조번호[유효기간] 회수사유 디아이디바이오
카슈트현탁액
23082[2026-12-17]
품질부적합(미생물한도)
- 의약품 회수 알림- 오마코 연질캡슐(건일)
1. 본원에서 사용중인 오마코 연질캡슐(건일) 에 대한 의약품 회수 사실안내 입니다.
2. 일부 제조번호에서시판 후 안정성시험에서 과산화물가결과 기준 초과로 인한 영업자 회수입니다.
3. 회수대상 의약품의 제조번호 [유효일자] 는 다음과 같습니다
4. 다른 제조번호 제품의 경우 문제 없이 사용 가능합니다.
업체명 제품명 제조번호[제조일자] 회수사유 건일제약
오마코연질캡슐
22001 /2022.01.06
시판후 안정성시험에서 과산화물가결과 기준 초과로 인한 영업자 회수
- 의약품 회수 알림- 듀로셉톨캡슐 30mg, 60mg
1. 본원에서 사용중인 듀로셉톨캡슐 30mg, 60mg 에 대한 의약품 회수 사실안내 입니다.
2. 일부 제조번호에서 불순물(N-nitroso-duloxetine) 초과 검출에 따른 사전예방적 조치로 시중 유통품에
대해 영업자 회수입니다.
3. 회수대상 의약품의 제조번호 [유효일자] 는 다음과 같습니다
4. 다른 제조번호 제품의 경우 문제 없이 사용 가능합니다.
업체명 제품명 제조번호[사용기한] 회수사유 환인제약 듀로셉톨캡슐30mg AN01AA[2024-12-31],
AP01AA[2026-02-28],
AP01BA[2026-02-28]불순물(N-nitroso-duloxetine) 초과 검출에 따른 사전예방적 조치로 시중 유통품에 대해 영업자 회수 환인제약 듀로셉톨캡슐60mg 650N01AA[2025-01-31],
AP01AA[2026-02-28],
AP01BA[2026-02-28]불순물(N-nitroso-duloxetine) 초과 검출에 따른 사전예방적 조치로 시중 유통품에 대해 영업자 회수
- 의약품 회수 알림- 트롬빅스정75mg(일동)
1. 본원에서 사용중인 트롬빅스정75mg(일동)에 대한 의약품 회수 사실안내 입니다.
2. 일부 제조번호에서 시판후 안정성 시험 중 기타 유연물질 기준 초과에 따른 영업자회수입니다.
3. 회수대상 의약품의 제조번호 [유효일자] 는 다음과 같습니다
4. 다른 제조번호 제품의 경우 사용 가능합니다
- 포타겔현탁액 20ml pack(대원) 품절 해제 건
회수조치로 일시 품절되었던 포타겔현탁액 20ml pack(대원) 의 새로운 제조번호 제품공급이 재개되어 일시 품절이 해제됨을 알려드리오니 참고하시기 바랍니다.
품절해제일 : 23.12.12
관련문의 : 약품관리실 (02-970-8384)
- 콘텐츠 담당자 : 약제부




